[ЕМЖС]УРЙњЗбГЧЖљЭЏвНдКПЦбЇМвЭЈЙ§ЖЏЮяЪЕбщЃЌРћгУвЛжжЙиМќЕААзжЪРДЕїНкЙиМќУтвпЯИАћЙІФмЃЌДгЖјФмАВШЋПижЦжзСіЩњГЄЁЃбаОПШЫдБжИГіЃЌаТбаОПдкЖЏЮяЩэЩЯНјааЃЌЩаЮДзМБИКУШЫРрСйДВВтЪдЁЃ
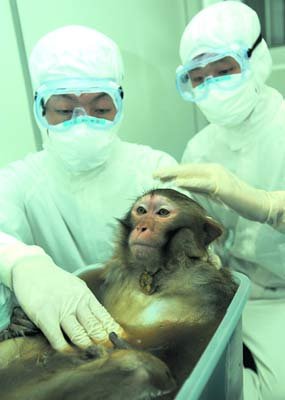
ОнЮяРэбЇМвзщжЏЭјНќШеБЈЕРЃЌУРЙњЗбГЧЖљЭЏвНдКПЦбЇМвЭЈЙ§ЖЏЮяЪЕбщЃЌРћгУвЛжжЙиМќЕААзжЪРДЕїНкЙиМќУтвпЯИАћЙІФмЃЌДгЖјФмАВШЋПижЦжзСіЩњГЄЁЃбаОПШЫдБжИГіЃЌИУбаОПжЄУїСЫгУвЉЮяРДЕїНкЬиЪтУтвпЯИАћЃЌАВШЋдіНјУтвпЛњФмПижЦжзСіЩњГЄЪЧПЩФмЕФЃЌвдДЫЮЊЛљДЁЃЌгаЭћЮЊАЉжЂУтвпСЦЗЈПЊЗЂГіаТвЉЮяЁЃЯрЙиТлЮФЗЂБэдкзюНќГіАцЕФЁЖздШЛ·вНбЇЁЗЩЯЁЃ
ЁАУтвпбЇжагаИіЛљБОЕФУЌЖмЃКЮЊКЮУтвпЯЕЭГВЛФмдквЛПЊЪМОЭдЄЗРАЉжЂЃПЁБбаОПИКд№ШЫЁЂЗбГЧЖљЭЏвНдКвЦжВУтвпбЇЗжВПвНбЇВЉЪПЮЄЖї·ККПМПЫЫЕЃЌД№АИЪЧИДдгЕФЃЌЕЋжївЊЩцМАЕНУтвпЯЕЭГИївђЫижЎМфЕФОЋУмЦНКтЃКУтвпЯЕЭГБЃЛЄЩэЬхЕжПЙМВВЁЃЌЕЋЙ§ЖШЛюдОгжЛсв§ЗЂздЩэУтвпЃЌгаЪБЩѕжСЛсДјРДЩњУќЮЃЯеЃЛЙ§гкЕЭУддђВЛзувдБЃЛЄЩэЬхЖдПЙМВВЁЁЃШчЙћФмОЋаФЕїНкЙиМќУтвпЯИАћЙІФмЃЌОЭгаЭћПЊЗЂГівЛжжШЋаТЕФжзСіУтвпСЦЗЈ——РћгУздЩэУтвпЯЕЭГРДЙЅЛїжзСіЁЃвЊзіЕНетвЛЕуЃЌУтвпЯЕЭГБиаывЊМШФмЫѕаЁжзСіЃЌгжВЛЛсДЅЗЂВЛЦкЭћЕФздЩэУтвпЗДгІЁЃ
баОПЕФжиЕуЪЧвЛжжУћЮЊFoxp3+TregsЕФУтвпЯИАћбЧаЭЁЃШЫУЧвбжЊTregsЃЈT-regulatoryЃЉОпгавжжЦУтвпЗДгІЕФЙІФмЃЌЕЋЫќвдМѕШѕЖджзСіЕФУтвпЗДгІЮЊДњМлЁЃЁАЮвУЧашвЊевЕНвЛжжЗНЗЈЃЌвдФГжжЗНЪНМѕШѕTregЕФЙІФмЃЌдЪаэПЙжзСіЗДгІЃЌгжВЛЛсв§ЗЂздЩэУтвпЗДгІЁЃЁБККПМПЫЫЕЁЃ
баОПЯдЪОЃЌвжжЦУИp300ФмгАЯьСэвЛжжУћЮЊFox3ЕФЕААзжЪЕФЙІФмЃЌетжжЕААздкПижЦTregsЕФЩњЮяадФмЗНУцЦ№зХживЊзїгУЁЃЫћУЧЗЂЯжЃЌШчЙћЩОГ§аЁЪѓЬхФкБэДяp300ЕФЛљвђЃЌОЭФмАВШЋЕиМѕШѕTregЕФЙІФмЃЌЯожЦжзСіЩњГЄЁЃЖјЧвЃЌгУвЛжжФмвжжЦp300ЕФвЉЮядке§ГЃаЁЪѓЩэЩЯвВФмгАЯьp300КЭTregsЙІФмЃЌгыЩОГ§ЛљвђЕФаЇЙћЯрЭЌЁЃ
TregОпгаЫЋЯђЕїНкЕФЙІФмЃЌЯђЯТЕїНкЛсдіНјУтвпЗДгІЃЌШУУтвпЯЕЭГЙЅЛїВЛЪмЛЖгЕФЭтРДепЃЌБШШчжзСіЃЛЯђЩЯЕїНкдђвжжЦУтвпЗДгІЃЌПЩвдМѕЩйЛњЬхХХГтЁЃ2007ФъбаОПаЁзщдјНјааЙ§вЛЯюЖЏЮяЪЕбщЃЌдіЧПTregЙІФмвдвжжЦУтвпЗДгІЃЌФПЕФЪЧШУЩэЬхИќКУЕиШнШЬвЦжВЦїЙйЁЃдкетСНИіР§згжаЃЌЖМвРППСЫвЛжжЭтВПЙ§ГЬ——РћгУвЛжжНазіввѕЃЛљЭХЕФЛЏбЇЮяжЪРДаоИФЙиМќЕААзЃЌЕЋЪЧЗНЯђЯрЗДЁЃЁАетЪЧУтвпЯЕЭГЙІФмЕФвѕбєСНУцЁЃЁБККПМПЫЫЕЁЃ
баОПШЫдБжИГіЃЌаТбаОПдкЖЏЮяЩэЩЯНјааЃЌЩаЮДзМБИКУШЫРрСйДВВтЪдЁЃСйДВЧАбаОПЪЧвЛЯюдРэТлжЄЃЌетвЛГЩЙћЧаЪЕЕиЭЦНјСЫАЉжЂУтвпСЦЗЈЃЌгаЭћзЊЛЏЮЊСйДВгІгУЁЃЫћУЧЛЙНЋЖдp300дкУтвпСЦЗЈжаЕФзїгУзіНјвЛВНбаОПЁЃ



 НвУигЁЖШЩњвтзюЛ№БЌЕФДњдаЙЄГЇ
НвУигЁЖШЩњвтзюЛ№БЌЕФДњдаЙЄГЇ ГцВнжаЬэМгЁАЮАИчЁБЃПзЈМвГЦЮоМьбщвРОн
ГцВнжаЬэМгЁАЮАИчЁБЃПзЈМвГЦЮоМьбщвРОн Л№ЙјЁЂаЁСњЯКдНГддНЯыГдЃП ЕиВЭЙнЕїСЯМь
Л№ЙјЁЂаЁСњЯКдНГддНЯыГдЃП ЕиВЭЙнЕїСЯМь ЪЕХФИОПЦЪЕЯАШЋГЬЃКХЎШЫдНЦЏССдНШнвзЕУ
ЪЕХФИОПЦЪЕЯАШЋГЬЃКХЎШЫдНЦЏССдНШнвзЕУ гЂХЎзгЕУСЫЁАЫЏУРШЫжЂЁБ УПЬьЧхабСНаЁЪБ
гЂХЎзгЕУСЫЁАЫЏУРШЫжЂЁБ УПЬьЧхабСНаЁЪБ


 Б№ЖдМВВЁЕФаЁаХКХЪгЖјВЛМћ
Б№ЖдМВВЁЕФаЁаХКХЪгЖјВЛМћ УРШнОѕПЩвдИФЩЦСГЩЋ Дђї§ШДШУФуРЯГѓБП
УРШнОѕПЩвдИФЩЦСГЩЋ Дђї§ШДШУФуРЯГѓБП ХЬЕуШщЗПЬЋДѓЖдХЎШЫДјРДЕФНЁПЕЮЃКІ
ХЬЕуШщЗПЬЋДѓЖдХЎШЫДјРДЕФНЁПЕЮЃКІ ѓПЫкПЧГдСЫгаЪВУДИаОѕ
ѓПЫкПЧГдСЫгаЪВУДИаОѕ гЂЙњЭбХЗЃЌЖдЮвЙњгЊбјБЃНЁВњвЕЕФгАЯь
гЂЙњЭбХЗЃЌЖдЮвЙњгЊбјБЃНЁВњвЕЕФгАЯь ЮэіВЯТЕФздОШЗНАИЃЈ2017АцЃЉ
ЮэіВЯТЕФздОШЗНАИЃЈ2017АцЃЉ ШјЕТЖджаЙњБЃНЁЪГЦЗЕФНјГіПкгаКЮгАЯь
ШјЕТЖджаЙњБЃНЁЪГЦЗЕФНјГіПкгаКЮгАЯь ШеБОКЫЗјЩфЕиЧјЩњВњЕФЪГЮяГдСЫдѕУДАь
ШеБОКЫЗјЩфЕиЧјЩњВњЕФЪГЮяГдСЫдѕУДАь H7N9ВЁЖОжаЛАМІШт ВњвЕАВШЋДйЗЂеЙ
H7N9ВЁЖОжаЛАМІШт ВњвЕАВШЋДйЗЂеЙ ГЄШ§НЧгЊбјБЃНЁВњвЕСЊУЫаХЯЂзЈБЈЃЈ3.15
ГЄШ§НЧгЊбјБЃНЁВњвЕСЊУЫаХЯЂзЈБЈЃЈ3.15









